Таргетная терапия при раке молочной железы препараты какой лучше
Содержание
Таргетная терапия рака молочной железы (РМЖ): что такое в онкологии, эффективность, последствия

При диагностировании онкологического заболевания груди женщинам назначается разностороннее лечение, включающее в себя проведение химио-и лучевой терапии, которые применяются с той целью, чтобы уничтожить злокачественные клетки в организме и предотвратить их дальнейшее распространение. Данные методы отрицательно воздействуют не только на атипичные, но и на здоровые клеточные структуры. Для улучшения переносимости такого вида лечения часто применяется таргетная терапия (ТГ).
Что такое
Таргетная терапия при раке молочной железы (РМЖ) представляет собой новую методику при лечении онкозаболеваний груди. Техника заключается в применении препаратов, которые оказывают точечное воздействие на изменившиеся клеточные структуры. Также данный вид еще называют иммунной таргет-терапией или молекулярной.
Благодаря использованию такой разновидности лечения появляется возможность воздействовать только на опухолевые клетки. При этом здоровые ткани не подлежат негативным изменениям. Именно благодаря такому эффекту побочные действия в ходе проведения терапевтических мероприятий возникают в редких случаях.
Препараты таргетной группы могут назначаться как самостоятельно, так и в совокупности с другими методиками, использующимся при выявлении онкологической патологии молочных желез. Кроме того, такие медикаментозные средства могут применяться в профилактических и лечебных целях по отношению к пациенткам, у которых отмечается распространение метастазов на отдаленные анатомические структуры.
Воздействие таргетных медикаментов направлено на внутриклеточные и наружные рецепторы, кровеносные сосуды, которые разрастаются вокруг опухолевого образования, а также на белки, участвующие в процессе выработки раковых клеток. Именно благодаря терапевтическому воздействию на эти мишени происходит гибель атипичных клеточных элементов.Также отмечается, что больные в большинстве случаев таргетную терапию при РМЖ переносят значительно легче, чем, например, гормоно- или химиотерапию. Также отмечено, что возникновение побочных эффектов при таком методе лечения отмечается только в 4% случаев онкозаболеваний раком груди.
Если применять данную методику совместно с химиотерапевтическим способом в борьбе со злокачественным процессом, то можно достичь максимально положительного терапевтического результата.
Препараты
Таргетная терапия в онкологии при поражении молочных желез подразумевает применение различных групп медикаментозных средств. Благодаря таким методам удается в течение длительного времени сдерживать распространение опухолевого образования или снизить в нем концентрацию раковых клеточных структур.
Такая тактика, несмотря на то что полностью не излечивает, позволяет перевести онкопроцесс из агрессивной формы в более вялотекущую.
Все агенты, используемые в ходе лечения, классифицируются на три большие группы.
Как правило, выделяют средства, негативное действие которых направлено на уничтожение так называемых мишеней. Это могут быть анти-HER2 препараты или антиэстрогены.
Кроме того, выделяют медикаменты, улучшающие среду, в которой формируется злокачественное новообразование. Например, могут применяться антиангиогенные медикаменты.
В третью категорию входят препараты, которые способствуют подавлению передачи сигналов внутри атипичных клеточных структур. Стоит сразу отметить, что многие таргент-агенты еще находятся на стадии исследования.
Создание всех медикаментозных средств направлено на то, чтобы максимально подавить мутирование ДНК-клеток, а также на остановку процесса формирования новых уплотнений.
Благодаря действию таких агентов происходит блокирование дальнейшего роста опухоли, что предотвращает увеличение очага поражения и распространение метастазов.
Выбор применения препаратов основывается на степени сложности патологии, индивидуальных особенностях женского организма и прочих составляющих.
Основная задача таргетных средств направлена на контроль генов, которые могут спровоцировать размножение онкологических клеточных структур, апоптоз и уничтожение атипичных клеток, блокировку выработки гормонов, способствующих роту образования, на закрытие доступа к здоровым анатомическим структурам, чтобы предупредить развитие новых опухолей.
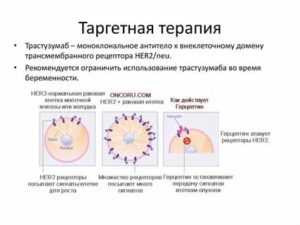
Анти-HER2-терапия
Для расшифровки используется такой термин, как рецептор второго типа к молекуле ростового эпидермального фактора. Основная его особенность заключается в распознавании им множественных сигналов, которые могут поступать от молекул, активирующих рост.
При появлении большого количества таких рецепторов прогноз выживаемости значительно ухудшается и в большинстве случаев возникают частые рецидивы патологического процесса. Чтобы этого не произошло, одни только стандартных методов лечения бывает недостаточно. С этой целью и применяется данный тип блокаторов.
Пертузумаб
Относится к новым препаратам, действие которых направлено на блокирование сразу нескольких сигналов, которые могут проходить через рецепторы.
Благодаря исследованиям было доказано, что данное средство целесообразно использовать в случае отрицательного результата от других медикаментов, в частности, Герцептина. Однако для достижения максимального эффекта рекомендуется одновременное назначение этих двух средств.
Также стоит отметить его хорошую переносимость пациентками и отсутствие токсического воздействия на сердечную систему.
Герцептин
До настоящего времени механизм его действия так и не был окончательно изучен. Однако есть предположение, что гибель раковых клеток происходит по принципу действия антител.
Эффективность от использования Герцептина отмечается и при раке метастатического типа, а также при наличии большого числа рецепторов HER2. Лучшие результаты от применения такого препарата отмечаются у людей, которым ранее не проводились никакие терапевтические мероприятия (35%). Положительный эффект у женщин, проходящих химиотерапию, отмечается только в 15 процентах случаев.
Использование средства показывает хорошие результаты как при самостоятельном применении, так и в комбинации с другими медикаментами.
Кроме того, эффективность Герцептина отмечается при HER2-позитивном раке, вне зависимости от стадии его развития, а также перед радиотерапией или хирургическим вмешательством, что позволяет сократить объем проведенных оперативных работ.Представляет собой моноклональные антитела. Благодаря прикреплению к белку роста замедляется процесс распространения злокачественных клеточных структур, в которых присутствует превышенная норма этого вещества.
В зависимости от степени тяжести течения онкозаболевания, данный препарат может применяться раз в семь дней или в более высокой дозировке – каждый 21 день. В организм лекарственное средство попадает посредством внутривенного введения.
Часто такой препарат назначается поле проведения операции по удалению опухоли груди, что способствует предотвращению повторного появления патологии.
Адо-трастузумаб эмтансин
Относится к группе конъюгатов антитело-лекарств, в состав которых входят моноклональные антитела, содержащиеся в химиопрепарате DM-1 и герцептине. Доставка медикамента происходит непосредственно к опухолевым клеткам.
Используется лекарственное средство при выявлении РМЖ распространенного типа. Как правило, инъекции вводят через каждые 21 день. Среди побочных эффектов может наблюдаться мышечная боль, приступы тошноты, повышенная усталость, снижение концентрации тромбоцитов в крови, нарушение стула в виде запоров и головные боли.
Не исключается развитие более серьезных проявлений, таких как аллергия, проблемы с сердцем, легкими и печенью.
Лапатиниб
Его действие также направлено на белок роста. Применяется при распространенном HER2-положительном онкологическом заболевании грудной железы, когда при помощи Трастузумаба или химиопрепаратов положительного результата достичь не удалось.
Выпускается в виде таблеток, можно комбинировать с Летрозолом и Кселодой.
Для достижения максимальной эффективности рекомендуется использовать его одновременно с Трастузумабом.
Антиангиогенная таргетная терапия
В большинстве случаев применяется Бевацизумаб, который относится к моноклональным антителам. Через 6 месяцев его использования отмечается уменьшение плотности сосудов в злокачественном образовании.
Однако, после отмены повторный неоангиогенез усиливается. На основании таких результатов многие специалисты пришли к выводу, что лечение данным медикаментом должно быть длительным.
Анти-PARP-препараты
Одним из наиболее распространенных лекарств является Инипариб. Несмотря на то что он до сих пор еще проходит клинические исследования, было отмечено, что в результате его применения происходит снижение скорости прогрессирования высокозлокачественных опухолей и увеличение продолжительности жизни больных.
Показания
Таргетная терапия РМЖ применяется в следующих случаях:
- последняя стадия онкологической болезни;
- крайне тяжелое состояние больной;
- невозможность проведения хирургического вмешательства;
- высокий риск развития осложнений после операции;
- вероятность распространения метастазов.
Кроме того, лечение таргетными препаратами назначается в тех ситуациях, когда отмечается быстрое размножение атипичных клеточных структур.
Противопоказания
Несмотря на высокую эффективность от применения такой тактики терапевтических мероприятий по устранению ракового процесса, данный метод имеет определенные ограничения к проведению.
Использовать ТГ запрещено в период вынашивания ребенка и кормления грудью, по отношению к детям, не достигшим 18-летнего возраста.
Кроме того, таргетная терапия противопоказана при повышенной чувствительности к компонентам применяемых медикаментозных средств.
Плюсы терапии
Среди основных преимуществ данного вида лечения выделяют прежде всего тот момент, что применять его можно не только на начальных этапах формирования злокачественного новообразования, но также и при процессе метастазирования. Кроме того, таргетная терапия возможна при противопоказаниях к использованию химиотерапии.
Также к положительным сторонам относят минимальное проявление побочных действий, хорошую переносимость пациентками, снижение рисков распространения опухоли на вторую молочную железу и повторное развитие болезни, повышение продолжительности жизни больных.
Также стоит отметить, что при таком подходе отсутствует необходимость корректировать концентрацию гемоглобина в организме.
Побочные эффекты
Несмотря на большое количество плюсов тергетного вида лечения, при данной тактике не исключается появление некоторых осложнений.
Чаще всего отмечается лихорадка и озноб, что можно устранить при помощи нестероидных медикаментозных средств противовоспалительного характера.
Среди более серьезных последствий выделяют нарушение работы сердца и сердечную недостаточность.
Эффективность
В целом таргетная терапия при РМЖ позволяет достичь высоких положительных результатов от лечения. Кроме того, отмечается увеличение сроков выживаемости больных.
Применение таргетных препаратов при диагностировании рака молочных желез является новым методом в борьбе с онкологическим заболеванием.
Методика обладает рядом преимуществ в сравнении с химиотерапией и иммунотерапией и вызывает минимум побочных эффектов. Однако нужно не забывать, что ТГ имеет определенные противопоказания к применению.
Поэтому перед началом лечения необходимо пройти полное диагностическое обследование.
Источник: https://onkologia.ru/onkomammologiya/targetnaya-terapiya-raka-molochnoy-zhelezy/
Принцип таргетной терапии рака молочной железы, применяемые препараты и эффективность
Лечение рака молочной железы заключается в удалении массива злокачественных клеток, которая могла быть до этого уменьшена в размерах с помощью лучевой терапии или специальных препаратов (химиотерапия и гормонотерапия), с последующей профилактикой рассевания злокачественных клеток по кровеносному или лимфатическому руслу.
К сожалению, как химиотерапия, так и облучение различными изотопами, необходимые для профилактики рецидивирования и метастазирования карциномы, являются токсичными для организма методами. Улучшить их переносимость можно, если дополнять лечение препаратами, не действующими на здоровые клетки. На это рассчитана появившаяся не так давно методика – таргетная терапия рака молочной железы.
Суть методики
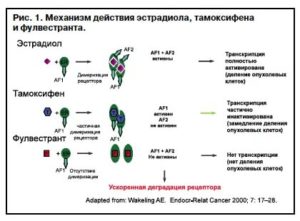
К 90-м годам двадцатого века ученые открыли и изучили большинство ключевых механизмов, регулирующих деление и выживаемость раковых клеток. Стало известно, что на их поверхности имеются особые рецепторы, сигнал от которых «включает» специфические ферменты и химические вещества, и таким образом карцинома постоянно растет, обходит иммунную защиту и может метастазировать.
Структур подобного строения в здоровых клетках нет. То есть, если организовать «адресную доставку» конкретно к опухолевым составляющим, можно остановить прогрессирование карциномы. Именно в этом и состоит суть таргетной терапии («таргет» в переводе с английского означает «мишень»).
Подобный вид лечения рака молочной железы является особым подвидом медикаментозной терапии, и может применяться как вместе с препаратами для «классической» химиотерапии, так и без них. Таргетная терапия не предполагает отказ от лучевой терапии или операции.
Большинство препаратов, применяемых для таргет-лечения, не уничтожают клетки карциномы молочной железы. Они подавляют механизмы, благодаря которым:
- или отдается команда к их делению;
- или ранее блокировалась их дифференцировка, из-за чего опухоль была менее дифференцированной, то есть – более быстро делящейся и злокачественной.
Виды таргетных агентов
Препараты для таргетной терапии при раке молочной железы позволяют длительно сдерживать рост опухоли или уменьшить массу находящихся в ней клеток. Такой перевод рака из крайне агрессивного и непредсказуемого состояния в хоть и злокачественное, но вялотекущее заболевание, является целью не худшей, чем полное излечение.
Агенты таргет-терапии, одобренные для лечения маммарной карциномы, разделяют на три больших группы:
- Средства, направленные на определенные «таргеты»-мишени. Это, например, антиэстрогены или анти-HER2-средства: Герцептин, Лапатиниб.
- Препараты, которые должны ухудшить условия существования опухоли. Это, к примеру, антиангиогенные средства (ангиогенез – это развитие новых сосудов, в частности, внутри опухоли).
- Лекарства, подавляющие передачу сигнала внутри массы раковых клеток. Большинство таргет-агентов еще проходят фазы клинических исследований.
Большинство данных препаратов относятся к классу моноклональных антител. Это молекулы, идентичные тем, которые образуются при вторжении в организм чужеродного агента.
Плюсы таргетной терапии
Применение подобного лечения:
- оптимально на ранних стадиях патологии, но также приносит хорошие результаты таргетная терапия, проводимая при раке молочной железы с метастазами;
- возможно, когда противопоказана химиотерапия;
- позволяет избежать коррекции уровня гемоглобина;
- обладает минимальными побочными действиями;
- в сочетании со стандартными видами терапии санкционирует значительное снижение риска появления подобной же опухоли после ее удаления и облучения ложа;
- увеличивает процент выживаемости.
Trastuzumab-DM1
Это средство представляет собой смесь Герцептина с производным другого препарата – Мэйтензина. Оно совмещает анти-HER2-воздействие и одновременную доставку токсичного для раковой клетки вещества непосредственно к ней.
Плюсом таргетной терапии Trastuzumab-DM1 является его эффективность в монотерапии, без препаратов для классической химиотерапии, что улучшает переносимость.
В настоящее время сравнивается эффективность этого средства с комбинациями других таргетных препаратов, применяемых в случае, когда при мспользовании Герцептина наблюдается прогрессирование рака.
Таргетная терапия при раке молочной железы

Таргетная терапия при раке молочной железы предполагает использование препаратов с анти-HER2-агентамитами, анти-PARP-агентами или антиангиогенами.
Такие средства наносят точечные удары только по опухолям, не затрагивая при этом здоровые. Именно поэтому лечение этими лекарствами легче переносится, чем использование лучевой или химиотерапии. Но самый главный плюс – эффективность.
Периоды ремиссии – в 3–4 раза дольше, чем после использования стандартных методов лечения РМЖ.
Принципы методики
Раковые клетки обладают специфичными рецепторами, сигнал от которых стимулирует выработку нужных для роста опухоли химических веществ. Чем активнее работает эта рецепторная система, тем успешнее раковые образования будет обходить иммунную защиту человека и быстрее начнут метастазировать.
Злокачественные клетки, образующиеся в молочной железе, имеют три рецепторные системы: HER-2/neu (erbB2), VEGF или ER.
В зависимости от того, какой вид преобладает в злокачественных опухолях, формируется один из трех типов рака груди – эстрогензависимый, прогестеронзависимый или херегулиновый (неврегулиновый).
Последняя разновидность является самой агрессивной (то есть патологически экспрессированной, быстро растущей).В здоровых клеточных структурах перечисленные выше системы отсутствуют, поэтому препараты, блокирующие работу раковых рецепторов, способны остановить развитие опухоли. На этом и основано действие препаратов, используемых в таргетной терапии (ее еще называют «прицельной» или «целевой»).
Преимущества таргетной терапии
Использование препаратов целесообразно и на начальных, и на последних стадиях рака. Например, таргетная терапия позволяет замедлить рост опухолей в молочных железах с метастазами и продлить жизнь пациентки на 10–12 месяцев больше, чем после традиционной химио- и лучевой терапии. Другие преимущества:
- Побочные эффекты менее мучительные, чем при использовании других методов лечения рака молочной железы.
- Возможно применение при противопоказаниях к химиотерапии, лучевой терапии, операции.
- Наименьший процент рецидирования при прохождении регулярных курсов (повторять их надо 10–12 раз в год в зависимости от применяемого препарата).
Основной минус в том, что применяемые в таргетной терапии препараты не включены в льготную программу лечения, заплатить за средства придется немалую сумму. Покупка лекарств на год обойдется минимум в 850 тыс. рублей.
Авастин
Основное показание – рецидивирующий или метастатический рак молочной железы HER-2-позитивного типа. Главное действующее вещество в составе – бевацизумаб (Bevacizumab).
Применяется в комбинации с Иринотеканом, Фторурацилом и Лейковорином.
Такое сочетание позволяет продлить жизнь пациенток с последними стадиями онкологии на 10–13 месяцев (тогда как только одна химиотерапия дает результат в 3 раза меньше).
Стандартная дозировка средства – 7,5 мг/кг каждые 3 недели. При агрессивном росте раковых опухолей – 10–15 мг/кг каждые 2 недели. При переходе в стадию ремиссии доза может быть снижена до 5 мг/кг. Стоит препарат от 35700 руб. за коробку с 16 флаконами.
Таргетная терапия при раке молочной железы препараты какой лучше
Современные методы борьбы с онкологией зарекомендовали свою эффективность. Таргетная терапия рака молочной железы основана на чувствительности клеток этого злокачественного новообразования к гормональным веществам.
Препараты, ориентированные на тропность клеточных структур опухоли к ним, быстро достигают целевого участка и воздействуют на онкопроцесс на молекулярном уровне.
Таргетные медикаменты имеют множественные побочные эффекты, отражающиеся на дыхательной, сердечно-сосудистой, нервной системе и желудочно-кишечном тракте.
Показания к проведению
Таргетное лечение применяется не только при раке молочной железы, но и при опухолях других локализаций. Но в случае опухоли груди показаниями к приему препаратов этой группы являются следующие клинические симптомы и данные лабораторных и инструментальных исследований:
- Уплотнение в молочной железе. Оно может быть обнаружено самой пациенткой или доктором женской консультации при диспансерном осмотре.
- Изменения в области соска. При опухолях молочных желез этот участок приобретает вид лимонной корки. Сам сосок часто втягивается.
- Наличие при ультразвуковом исследовании гиперэхогенных или анэхогенных участков. Эти данные свидетельствуют об аномальных уплотнениях паренхимы органа.
- Присутствие на снимках компьютерной и магнитно-резонансной томографии новообразований в характерных регионах железы.
- Обнаружение в крови специфических онкологических маркеров.
- Стремительное снижение веса пациентки. Опухоль, отбирающая из кровеносного русла питательные вещества, быстро истощает организм.
- Ухудшение биохимических показателей крови. В кровеносном русле растет концентрация трансаминаз — аланинаминотрансферазы, аспартатаминотрансферазы и щелочной фосфатазы.
- Появление водянистых или кровянистых выделений из соска.
Методика применения
Перед началом противоопухолевой терапии таргетными препаратами необходима постановка пробы на экспрессию опухолевых генов. Все описанные медикаменты вводятся внутривенно и капельно. Противопоказано доставлять эти лекарства в сосудистое русло струйно или болюсно.
Игнорирование этого правила влечет за собой тяжелые осложнения вплоть до летального исхода. Медикаменты можно использовать отдельно, в виде монотерапии или в комбинации с другими химиотерапевтическими средствами. Выделяют нагрузочные и поддерживающие дозы. Их рассчитывают на килограмм массы тела пациента.
При введении препарата нужно контролировать инфузионную реакцию для исключения анафилактического шока.
Противопоказания к приему
Противоопухолевые медикаментозные средства противопоказано принимать пациентам с гиперчувствительностью к ним.
Если у больных диагностирована чувствительность к белкам клеток яичников китайского хомяка, это также является прямым противопоказанием к приему лекарств, поскольку последние изготовляются с использованием этих протеинов. Нежелательно вводить лекарства, если пациенты уже получают антрациклины.
Эти медикаменты являются антагонистами. Еще одним противопоказанием считается сильная одышка в состоянии покоя, обусловленная метастазированием в легкие или сопутствующими сердечно-сосудистыми патологиями.
